
Le nitrate de potassium
À propos de ce écoles sélection Wikipedia
SOS Enfants, un organisme de bienfaisance de l'éducation , a organisé cette sélection. Avec enfants SOS vous pouvez choisir de parrainer des enfants dans plus de cent pays
| Le nitrate de potassium | |
|---|---|
 | |
Autres noms Nitrate de potasse, Vesta poudre, ou | |
| Identificateurs | |
| Numéro CAS | 7757-79-1 |
| Propriétés | |
| Formule moléculaire | KNO 3 |
| Masse molaire | 101.1032 |
| Apparence | solide blanc |
| Densité | 2,109 g · cm -3 (16 ° C) (solide |
| Point de fusion | 334 ° C |
| Point d'ébullition | 400 ° C décomposition. |
| Risques | |
| FS | MSDS externe |
| Classification UE | O |
| Phrases-R | 8 |
| Phrases S | 17, 24/25 |
| NFPA 704 |  0 1 3 OX |
| Des composés apparentés | |
| D'autres anions | Nitrite de potassium |
| D'autres cations | nitrate de lithium Le nitrate de sodium nitrate de rubidium nitrate de césium |
| Page de données supplémentaire | |
| Structure et propriétés | n, ε r, etc. |
| Thermodynamique données | comportement de phase Solide, liquide, gaz |
| Les données spectrales | UV, IR, RMN , MS |
| Sauf indication contraire, les données sont données pour le matériel dans leur état standard (à 25 ° C, 100 kPa) | |
| Références d'Infobox | |
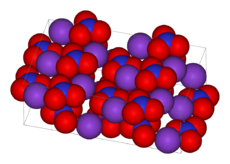
Le nitrate de potassium est un composé chimique avec la formule chimique K N O 3. Une source minérale d'origine naturelle de l'azote , KNO 3 constitue une critique composant oxydant de la poudre noire poudre . Dans le passé, il a également été utilisé pour plusieurs types de fusibles qui brûlent, y compris matchs lents. Depuis nitrate de potassium facilement précipite, urine était une source importante, par divers moyens malodorants, de la Fin du Moyen Age et Époque moderne à travers le 19ème siècle.
Ses noms communs comprennent le salpêtre, de Medieval petrae sal latine: «sel de pierre" ou éventuellement "Sel de Petra "(salpêtre en anglais américain), de nitrate de potasse, et de nitre. Le nom de salpêtre du Chili est appliquée à nitrate de sodium, un composé azoté différent qui est également utilisé dans les explosifs et les engrais.
Description
Le nitrate de potassium est le composant oxydant de la poudre noire . Avant l'industriel à grande échelle fixation de l'azote par la Procédé Haber, principales sources de nitrate de potassium ont été les dépôts de cristallisation des murs de la grotte et l'assèchement des décomposition matière organique. Fumiers étaient une source particulièrement commune: l'ammoniac de la décomposition de l'urée et d'autres matières azotées serait subir une oxydation bactérienne pour produire le nitrate. Il a été et est également utilisé en tant que composant dans des engrais . Lorsqu'il est utilisé par lui-même comme engrais, il a un score de NPK 13-0-38 de (indiquant 13,9%, 0%, et 38,7% d'azote, de phosphore et de potassium, en masse, respectivement). Le nitrate de potassium était autrefois considérée induire l'impuissance, et est toujours répandu pour être dans les aliments institutionnelle (comme tarif militaire) comme un anaphrodisiaque; ces utilisations seraient inefficaces, car le nitrate de potassium n'a pas de telles propriétés. Toutefois, le nitrate de potassium et d'autres nitrates ne combattre avec succès la haute pression sanguine et sont utilisés médicalement pour soulager l'angine de poitrine.
Fabrication
Historiquement, nitre-lits ont été préparés en mélangeant fumier de cendres soit mortier ou de bois, la terre commune et des matières organiques comme la paille pour donner la porosité à un tas de compost généralement 1,5 mètres de haut par 2 mètres de large par 5 mètres de long. Le tas est généralement sous une couverture de la pluie, maintenu humide avec de l'urine, se souvent pour accélérer la décomposition et la lessivé à l'eau après environ un an. Le liquide contenant divers nitrates a été ensuite converti avec de la cendre de bois pour les nitrates de potassium, cristallisé et raffiné pour une utilisation dans la poudre à canon .
Dans une époque plus rurales, l'urine a été recueillie et utilisée dans la fabrication de la poudre. Vieille urine a été filtré à travers un tonneau plein de paille et a permis de continuer à se dégrader pendant un an ou plus. Après cette période de temps, de l'eau a été utilisé pour laver les sels chimiques résultant de la paille. Cette suspension a été filtrée à travers de la cendre de bois et on laisse sécher au soleil. cristaux de salpêtre ont ensuite été recueillis et ajoutés à Brimstone et charbon de bois pour créer la poudre noire .
Le nitrate de potassium peut aussi être récolté à partir d'accumulations de bat guano dans les grottes. Ce était la méthode traditionnelle utilisée au Laos pour la fabrication de la poudre à canon pour Bang Fai roquettes.
Pendant le 19ème siècle et jusque vers la Première Guerre mondiale , le nitrate de potassium a été produite à l'échelle industrielle, d'abord par la Birkeland-Eyde processus en 1905, puis plus tard de ammonium produit par le beaucoup plus efficace Procédé Haber. Ce dernier procédé est venu en ligne lors de la Première Guerre mondiale, et a fourni Allemagne avec nitrates critiques pour la guerre qui autrement ne avait pas accès parce que les dépôts de nitrate naturel au Chili étaient aux mains des Britanniques. Il est supposé que cette prolongé la Première Guerre mondiale Aujourd'hui pratiquement tous les nitrates sont produits par l'ammoniac du procédé Haber.
Applications
Salpêtre a été utilisé comme un anaphrodisiaque à travers l'histoire.
Le nitrate de potassium est aussi utilisé comme un engrais , en amateur propergol, et dans plusieurs feux d'artifice tels que fumer bombes, dans lequel un mélange de sucre produit un nuage de fumée de 600 fois leur propre volume. Le ratio des bombes de fumée utilisant le saccharose (sucre en poudre) et de nitrate de potassium est de 40 (C 12 H 22 O 11): 60 (KNO 3). Il peut être utilisé tel quel, ou consolidés en une masse en mélangeant avec de l'eau pour faire une pâte et laisser sécher pendant la nuit.
Dans le procédé de la conservation des aliments, le nitrate de potassium a été un ingrédient commun de la viande salée, mais son utilisation est déconseillée. Dans l'Union européenne, il est appelé E252.
Il est couramment utilisé dans les cigarettes préalablement laminée à maintenir un même brûler du tabac
Le nitrate de potassium est également le composant principal (habituellement environ 98%) de souche d'arbre décapant; il accélère la décomposition naturelle de la souche.
Il a également été utilisé dans la fabrication de la crème glacée et peut être trouvé dans certains dentifrices pour sensibles dents. Récemment, l'utilisation de nitrate de potassium dans dentifrices pour dents sensibles traitement a considérablement augmenté, en dépit du fait qu'il n'a pas été démontré de façon concluante pour aider hypersensibilité dentaire.
Le nitrate de potassium est également l'une des trois parties de la poudre noire , en même temps que le charbon de bois en poudre (sensiblement de carbone) et de soufre, où il agit comme un comburant.
Littérature
- Alan Williams: La production de salpêtre dans le moyen âge, Ambix, 22 (1975), p. 125-33. Maney Publishing, ISSN 0002-6980.
