
Sel (chimie)
Contexte des écoles Wikipédia
Enfants SOS ont produit une sélection d'articles de wikipedia pour les écoles depuis 2005. Cliquez ici pour plus d'informations sur les enfants SOS.

Un sel, en chimie , est défini comme le produit formé par la réaction de neutralisation des acides et bases. Les sels sont composés ioniques composés de cations (positivement chargés ions) et anions (ions négatifs), de sorte que le produit est électriquement neutre (sans charge nette). Ces composants peuvent être des ions inorganique tel que le chlorure (Cl -), ainsi que organique tel que acétate (CH 3 COO -), et ions monoatomiques tels que le fluorure (F -), ainsi que ions polyatomiques tels que le sulfate (SO 4 2-).
Il existe plusieurs variétés de sels. Les sels qui produisent hydroxyde ions dissous dans l'eau sont des sels basiques et des sels qui produisent ions hydronium dans l'eau sont des sels acides. sels neutres sont ceux qui ne sont ni acide, ni les sels basiques. Zwitterions contiennent un centre anionique et un centre cationique dans la même molécule , mais ne sont pas considérés comme des sels. Des exemples comprennent des acides aminés , de nombreux métabolites, peptides et protéines .
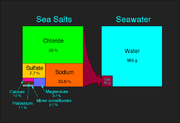
Lorsque les sels sont dissous dans de l'eau, on les appelle électrolytes, et sont en mesure de procéder à l'électricité , une propriété qui est partagée avec des sels fondus. Mélanges de nombreux différents ions en solution comme dans le cytoplasme des cellules , dans le sang , urine, la sève des plantes et Waters minérale habituellement ne font pas de sels définis après évaporation de l'eau. Par conséquent, leur teneur en sel est donnée pour les ions respectifs.
Propriétés

Couleur
Les sels peuvent semblent être claires et transparente ( chlorure de sodium ), opaque, et même métallique et brillante ( disulfure de fer ). Dans de nombreux cas, le apparentes ou l'opacité transparence ne est liée à la différence de taille de la personne monocristaux. Puisque la lumière est réfléchie par la joints de grains (limites entre cristallites), grands cristaux ont tendance à être transparent, tout en agrégats polycristallins ressemblent poudres blanches. Bien sûr, certains sels sont intrinsèquement opaque.
Sels existent dans différentes couleurs , par exemple, jaune (sodium chromate), orange ( le dichromate de potassium), rouge ( sulfure de mercure), mauve ( chlorure de cobalt hexahydraté), bleu ( sulfate de cuivre pentahydraté, hexacyanoferrate de fer), vert ( oxyde de nickel), incolore ( sulfate de magnésium), blanc, et noir ( du dioxyde de manganèse). La plupart des minéraux inorganiques et pigments ainsi que de nombreux organique synthétique les colorants sont des sels.
Goût
Différents sels peuvent susciter tous les cinq saveurs de base, par exemple salée ( chlorure de sodium ), doux ( le diacétate de plomb; mais qui provoquera saturnisme en cas d'ingestion), aigre ( bitartrate de potassium), amère ( sulfate de magnésium), et umami ou salé ( glutamate monosodique).
Odeur
Les sels d'acides forts et bases fortes (" sels solides ») sont non- volatile et inodore, tandis que les sels d'acides faibles ou soit des bases faibles (" sels faibles ») peuvent sentir après la acide conjugué (par exemple acétates comme l'acide acétique ( vinaigre) et des cyanures tels que le cyanure d'hydrogène ( amandes ) ou la base conjuguée (par exemple les sels d'ammonium tels que l'ammoniaque ) des ions composant. Que, décomposition partielle lente est habituellement accélérée par la présence d'eau, étant donné que hydrolyse est l'autre moitié de la équation de la réaction réversible de formation de sels faibles.
Nomenclature

Le nom d'un sel commence par le nom du cation (par exemple de sodium ou d'ammonium) suivi du nom de l'anion (par exemple un chlorure ou un acétate). Les sels sont souvent désignés uniquement par le nom du cation (par exemple sel de sodium ou d'ammonium, de sel) ou par le nom de l'anion (par exemple un chlorure ou un acétate).
Les cations formant des sels communs comprennent:
- ammonium NH 4 +
- calcium Ca 2+
- fer Fe 2+ et Fe 3+
- magnésium soit Mg 2+
- potassium K +
- pyridinium C 5 H 5 NH +
- quaternaire NR 4 + ammonium
- sodium Na +
Anions formant des sels communs (et le nom des acides parents entre parenthèses) comprennent:
- acétate CH 3 COO - ( acide acétique )
- carbonate CO 3 2- ( l'acide carbonique)
- chlorure Cl - ( acide chlorhydrique )
- HOC citrate (COO -) (CH 2 COO -) 2 ( acide citrique)
- cyanure C≡N - ( cyanure d'hydrogène )
- hydroxyde OH - ( eau )
- nitrate NO 3 - ( acide nitrique )
- NO nitrite 2 - ( l'acide nitreux)
- oxyde O 2- ( l'eau )
- phosphate PO 4 3- ( acide phosphorique )
- sulfate SO 4 2- ( acide sulfurique )
Formation
Les sels sont formés par une réaction chimique entre:
- Les sels peuvent également former si des solutions de sels différents sont mélangés, leurs ions se recombinent, et le nouveau sel est insoluble et précipités (voir: solubilité d'équilibre), par exemple:
Pb (NO 3) 2 (aq) + Na 2 SO 4 (aq) → PbSO 4 (s) + NaNO 3 (aq)
