
Radon
À propos de ce écoles sélection Wikipedia
SOS Enfants a essayé de rendre le contenu plus accessible Wikipedia par cette sélection des écoles. Les enfants SOS est le plus grand don de charité du monde enfants orphelins et abandonnés la chance de la vie familiale.
| Radon | ||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
Rn 86 | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| Apparence | ||||||||||||||||||||||||||||||||||
gaz incolore  | ||||||||||||||||||||||||||||||||||
| Propriétés générales | ||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | radon, Rn, 86 | |||||||||||||||||||||||||||||||||
| Prononciation | / r eɪ ré ɒ n / RAY -Don | |||||||||||||||||||||||||||||||||
| Élément Catégorie | gaz nobles | |||||||||||||||||||||||||||||||||
| Groupe, période, bloc | 18 (gaz rares) , 6, p | |||||||||||||||||||||||||||||||||
| Poids atomique standard | (222) | |||||||||||||||||||||||||||||||||
| Configuration électronique | [ Xe ] 4f 14 5d 10 6s 6p 2 6 2, 8, 18, 32, 18, 8 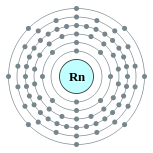 | |||||||||||||||||||||||||||||||||
| Histoire | ||||||||||||||||||||||||||||||||||
| Découverte | Friedrich Ernst Dorn (1898) | |||||||||||||||||||||||||||||||||
| Premier isolement | William Ramsay et Robert Whytlaw-Gray (1910) | |||||||||||||||||||||||||||||||||
| Propriétés physiques | ||||||||||||||||||||||||||||||||||
| Phase | gaz | |||||||||||||||||||||||||||||||||
| Densité | (0 ° C, 101,325 kPa) 9,73 g / L | |||||||||||||||||||||||||||||||||
| Liquid densité à BP | 4,4 g · cm -3 | |||||||||||||||||||||||||||||||||
| Point de fusion | 202,0 K , -71,15 ° C -96,07 ° C | |||||||||||||||||||||||||||||||||
| Point d'ébullition | 211,3 K, -61,85 ° C, -79,1 ° F | |||||||||||||||||||||||||||||||||
| Point critique | 377 K, 6,28 MPa | |||||||||||||||||||||||||||||||||
| La chaleur de fusion | 3,247 kJ · mol -1 | |||||||||||||||||||||||||||||||||
| Chaleur de vaporisation | 18,10 kJ · mol -1 | |||||||||||||||||||||||||||||||||
| Capacité thermique molaire | 5 R / 2 = 20,786 J · mol -1 · K -1 | |||||||||||||||||||||||||||||||||
| La pression de vapeur | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| Propriétés atomiques | ||||||||||||||||||||||||||||||||||
| États d'oxydation | 6, 2, 0 | |||||||||||||||||||||||||||||||||
| Électronégativité | 2,2 (échelle de Pauling) | |||||||||||||||||||||||||||||||||
| énergies d'ionisation | 1er: 1037 kJ · mol -1 | |||||||||||||||||||||||||||||||||
| Rayon covalente | 150 h | |||||||||||||||||||||||||||||||||
| Rayon de Van der Waals | 220 h | |||||||||||||||||||||||||||||||||
| Miscellanées | ||||||||||||||||||||||||||||||||||
| Crystal structure | cubique à faces centrées  | |||||||||||||||||||||||||||||||||
| Ordre magnétique | non magnétique | |||||||||||||||||||||||||||||||||
| Conductivité thermique | 3,61 m W · m -1 · K -1 | |||||||||||||||||||||||||||||||||
| Numéro de registre CAS | 10043-92-2 | |||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | ||||||||||||||||||||||||||||||||||
| Article détaillé: Isotopes de radon | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
Le radon est un élément chimique de symbole Rn et de numéro atomique 86. C'est un radioactif, incolore, inodore, insipide gaz noble , naturel comme un produit de désintégration indirecte de l'uranium ou le thorium . Son plus stable isotope , 222 Rn, a une demi-vie de 3,8 jours. Le radon est un des plus denses substances qui reste un gaz dans des conditions normales. Il est également le seul gaz dans des conditions normales qui ne dispose que des isotopes radioactifs, et est considéré comme un danger pour la santé en raison de sa radioactivité. Intense radioactivité a également entravé les études chimiques de radon et à seulement quelques composés sont connus.
Le radon est formée comme une étape intermédiaire de la normale radioactifs chaînes de désintégration, à travers lequel le thorium et l'uranium se désintègrent lentement dans le plomb . Thorium et l'uranium sont les deux éléments radioactifs les plus communs sur la terre; ils ont été autour depuis la terre a été formée. Leurs isotopes naturels ont de très longues demi-vies, de l'ordre de milliards d'années. Thorium et l'uranium, son produit de désintégration du radium , le radon et ses produits de désintégration, continueront donc à se produire pour des dizaines de millions d'années à peu près les mêmes concentrations comme ils le font maintenant. Comme le radon se désintègre lui-même, il produit de nouveaux éléments radioactifs dits de filiation du radon ou produits de désintégration. Contrairement au radon gazeux lui-même, de filiation du radon sont solides et collent aux surfaces, telles que des particules de poussière dans l'air. Si une telle poussière contaminée est inhalé, ces particules peuvent se coller sur les voies aériennes du poumon et augmenter le risque de développer un cancer du poumon.
Contrairement à tous les autres éléments intermédiaires dans les chaînes de désintégration ci-dessus, le radon gazeux et est donc facilement inhalé. Ainsi, même en cette ère de réacteurs nucléaires, le radon d'origine naturelle est responsable de la majorité de l'exposition du public aux rayonnement ionisant. Ce est souvent le plus gros contributeur à une personne de la dose de rayonnement d'arrière-plan, et est le plus variable d'un endroit à. Malgré sa courte durée de vie, un peu de gaz radon à partir de sources naturelles peut se accumuler à des concentrations beaucoup plus élevé que la normale dans les bâtiments, surtout dans les endroits clos tels que les greniers et les caves. Il peut également être trouvé dans certains les eaux de source et des sources chaudes.
Des études épidémiologiques ont montré un lien clair entre inhalation de fortes concentrations de radon et l'incidence de cancer du poumon . Ainsi, le radon est considéré comme un contaminant important qui affecte qualité de l'air intérieur dans le monde entier. Selon le Environmental Protection Agency, le radon est la deuxième cause la plus fréquente de cancer du poumon, après le tabagisme, provoquant 21 000 décès par cancer du poumon par an dans le États-Unis . A propos de 2900 de ces décès surviennent chez les personnes qui ne ont jamais fumé. Alors que le radon est la deuxième cause la plus fréquente de cancer du poumon, il est la première cause chez les non-fumeurs, selon les estimations de l'EPA.
Caractéristiques
Propriétés physiques
Le radon est un gaz incolore et inodore, et donc pas détectable par les seuls sens humains. À température et pression normales, le radon forme un gaz monoatomique avec une densité de 9,73 kg / m 3, à environ huit fois la densité de l' atmosphère de la Terre au niveau de la mer, 1,217 kg / m 3. Le radon est un des gaz les plus denses à température ambiante et est la plus dense des gaz nobles. Bien incolore à température et pression standard, lorsqu'il est refroidi en dessous de son point de congélation de 202 K (-71 ° C; -96 ° F), le radon émet une brillante radioluminescence qui passe du jaune au rouge-orange en tant que la température baisse. Sur la condensation, le radon se allume en raison de l'intense rayonnement qu'il produit.
Propriétés chimiques
Être un gaz noble, le radon est chimiquement peu réactif. Cependant, la demi-vie de 3,8 jours radon-222 rend utile dans les sciences physiques comme un élément naturel traceur.
Le radon est un membre des zéro- valence éléments qui sont appelés gaz nobles. C'est inerte à des réactions chimiques les plus courants, tels que la combustion, car la partie extérieure valence enveloppe contient huit électrons. Ceci produit une configuration stable, minimum d'énergie dans laquelle les électrons externes sont étroitement liés. 1037 kJ / mol est nécessaire pour extraire un électron à partir de ses coquilles (également connu sous le nom première énergie d'ionisation). Toutefois, conformément à l'évolution périodique , le radon a une plus faible électronégativité de l'élément une période antérieure, le xénon , et est donc plus réactif. Le radon est difficilement soluble dans l'eau, mais plus soluble que les gaz nobles légers. Le radon est sensiblement plus soluble dans les liquides organiques que dans l'eau. Les premières études ont conclu que la stabilité du radon hydrate doit être du même ordre que celle des hydrates de chlore (Cl 2) ou le dioxyde de soufre (SO 2), et significativement plus élevée que la stabilité de l'hydrate de de l'hydrogène sulfuré (H 2 S).
En raison de son coût et de la radioactivité, de la recherche expérimentale chimique est rarement réalisé avec le radon, et de ce fait il existe très peu de composés de radon signalé, tous soit fluorures ou oxydes. Le radon peut être oxydé par quelques agents oxydants puissants tels que le fluor , en formant ainsi difluorure de radon. Il se décompose en arrière à des éléments à une température supérieure à 250 ° C. Il a une faible la volatilité et a été pensé pour être RNF 2. Mais en raison de la courte demi-vie du radon et la radioactivité de ses composés, il n'a pas été possible d'étudier le composé en détail. Des études théoriques sur cette molécule prédire qu'il doit avoir une Rn-F longueur de la liaison de 2,08 Ǻ, et que le composé est thermodynamiquement plus stable et moins volatil que son homologue briquet XeF 2. Le molécule octaédrique RNF 6 a été prédit pour avoir une encore plus faible enthalpie de formation de la difluorure. Les fluorures supérieures rnf 4 et 6 RNF ont été revendiqués à exister, mais il est douteux qu'ils ont effectivement été synthétisés. Le [RNF] + ions est censé former par la réaction:
- Rn (g) + 2 [O 2] + [SbF 6] - (s) → [RNF] + [Sb 2 F 11] - (s) + 2 O 2 (g)
Oxydes de radon sont parmi les quelques autres signalé composés de radon; seul le trioxyde a été confirmée. Radon RNCO carbonyle a été prévu pour être stable et d'avoir un géométrie moléculaire linéaire. Les molécules Rn 2 et RnXe ont été trouvés significativement stabilisée par couplage spin-orbite. Radon l'intérieur d'une cage fullerène a été proposée comme un médicament pour tumeurs.
Isotopes

Radon n'a pas d'isotopes stables . Cependant, 36 les isotopes radioactifs ont été caractérisés, à leur masses atomiques allant de 193 à 228. L'isotope le plus stable est 222 Rn, qui est un la désintégration des produits de 226 Ra, un produit de désintégration de 238 U. Parmi les filles de 222 Rn est également l'isotope 218 Rn très instable.
Il ya trois autres isotopes du radon qui ont une demi-vie de plus d'une heure: 211 Rn, Rn 210 et 224 Rn. Le 220 Rn isotope est un produit de désintégration naturelle des plus stables du thorium isotope (232 Th), et est communément appelé thoron. Elle a une demi-vie de 55,6 secondes et émet également un rayonnement alpha. De même, 219 Rn est dérivé de l'isotope le plus stable de l'actinium (227 Ac) -named "actinon» -et est un émetteur alpha ayant une demi-vie de 3,96 secondes. Aucun isotopes du radon se produisent de manière significative dans le neptunium (237 Np) de la série de désintégration.
Descendances
Rn 222 appartient à la radium et de l'uranium-238 chaîne de désintégration, et a une demi-vie de 3,8235 jours. Ses quatre premiers produits (hors régimes de désintégration marginaux) sont de très courte durée, ce qui signifie que les désintégrations correspondants sont indicatifs de la distribution initial de radon. Sa décroissance passe par la séquence suivante:
- Rn 222, 3,8 jours, alpha décomposition à ...
- 218 Po , 3,10 minutes, alpha décomposition à ...
- 214 Pb , 26,8 minutes, beta décomposition à ...
- 214 Bi , 19,9 minutes, bêta décomposition à ...
- 214 Po, 0,1643 ms, alpha décomposition à ...
- 210 Pb, qui a une demi-vie de 22,3 années beaucoup plus longue, bêta décomposition à ...
- 210 Bi, 5,013 jours, bêta décomposition à ...
- 210 Po, 138,376 jours, alpha décomposition à ...
- 206 Pb, stable.
Le radon facteur d'équilibre est le rapport entre l'activité de tous les descendants du radon à courte période (qui sont responsables de la majorité des effets biologiques de radon), et l'activité qui serait à l'équilibre avec le parent du radon.
Si un volume fermé est constamment fourni avec le radon, la concentration d'isotopes de courte durée augmentera jusqu'à ce qu'un équilibre soit atteint où le taux de décroissance de chaque produit de désintégration sera égale à celle du radon lui-même. Le facteur d'équilibre est une lorsque les deux activités sont égaux, ce qui signifie que les produits de désintégration sont restés près de la parent assez longtemps pour que l'équilibre de radon à atteindre, d'ici quelques heures. Dans ces conditions, chaque tranche supplémentaire de pCi / L de radon augmenter l'exposition, de 0,01 WL (voir explication de WL ci-dessous). Ces conditions ne sont pas toujours respectées: dans de nombreux foyers, la fraction d'équilibre est généralement de 40%; ce est, il y aura 0,004 WL de la progéniture pour chaque pCi / L de radon dans l'air. 210 Pb est beaucoup plus longue (décennies) à venir en équilibre avec le radon, mais, si l'environnement permet l'accumulation de poussière sur de longues périodes de temps, 210 Pb et ses produits de désintégration peuvent contribuer à des niveaux de rayonnement global ainsi.
En raison de leur charge électrostatique, descendances radon adhèrent aux surfaces ou particules de poussière, alors que le radon gazeux ne est pas. Attachement les retire de l'air, ce qui provoque généralement le facteur d'équilibre dans l'atmosphère pour être inférieur à un. Le facteur d'équilibre est également abaissé au moyen de dispositifs de circulation d'air ou de filtration de l'air, et est augmenté par les particules de poussière en suspension, y compris la fumée de cigarette. En concentrations élevées, isotopes du radon dans l'air contribuent de manière significative au risque de la santé humaine. Le facteur d'équilibre trouvé dans les études épidémiologiques est de 0,4.
Histoire et étymologie

Le radon est l'élément radioactif cinquième à être découvert, en 1900 par Friedrich Ernst Dorn, après l'uranium, le thorium, le radium et le polonium. En 1900 Dorn signalé quelques expériences dans lesquelles il a remarqué que les composés de radium émanent un gaz radioactif qu'il nomma émanation de radium (Ra Em). Avant cela, en 1899, Pierre et Marie Curie ont observé que le «gaz» émis par le radium radioactifs est resté pendant un mois. Plus tard cette année, Robert B. Owens et Ernest Rutherford , au Université McGill, à Montréal , a remarqué variations en essayant de mesurer le rayonnement de l'oxyde de thorium. Rutherford a noté que les composés du thorium émettent en permanence un gaz radioactif qui conserve les pouvoirs radioactifs pendant plusieurs minutes, et a appelé cette émanation de gaz (de "emanare" latine -à écouler et "Emanatio" -expiration), et plus tard l'émanation du thorium (Th Em ). En 1901, il a démontré que les émanations sont radioactifs, mais les Curie crédité pour la découverte de l'élément. En 1903, des émanations similaires ont été observés à partir de l'actinium par André-Louis Debierne et ont été appelés Actinium Emanation (Ac Em).
Plusieurs noms ont été proposés pour ces trois gaz: exradio, exthorio et exactinio en 1904; le radon, du thoron et Akton en 1918; radeon, thoreon et actineon en 1919, et finalement le radon, du thoron et actinon en 1920. La ressemblance de les spectres de ces trois gaz avec ceux de l'argon, le krypton, et le xénon, et leur inertie chimique observée a conduit Sir William Ramsay suggérer en 1904 que les «émanations» peuvent contenir un nouvel élément de la famille des gaz rares.
En 1910, Sir William Ramsay et Robert Whytlaw-Gray isolé radon, déterminé sa densité, et a déterminé que ce était le gaz connue plus lourd. Ils ont écrit que «L'expression de l'émanation du radium is fort incommode", (l'expression d'émanation de radium est très maladroit) et a suggéré le nouveau nom niton (Nt) (des «nitens" latins signifiant "brillant") pour souligner la propriété radioluminescence, et en 1912 il a été accepté par la Commission internationale des poids atomiques. En 1923, le Comité international pour les éléments chimiques et Union internationale de chimie pure et appliquée (UICPA) choisi parmi les noms radon (Rn), thoron (Tn), et actinon (An). Plus tard, quand isotopes étaient comptés au lieu de son nom, l'élément prend le nom de l'isotope le plus stable, le radon, tandis que Tn a été renommé Rn 220 et An a été rebaptisé 219 Rn. Jusque dans les années 1960, l'élément a également été appelée simplement émanation. Le premier composé synthétisé du radon, le fluorure radon, a été obtenue en 1962.
Le danger d'une forte exposition au radon dans les mines, où les expositions atteignant 1.000.000 Bq / m 3 peut être trouvé, est connue depuis longtemps. En 1530, Paracelse décrit une maladie gaspiller des mineurs, l'metallorum mala, et Georg Agricola recommandé la ventilation dans les mines pour éviter ce mal des montagnes (Bergsucht). En 1879, cette condition a été identifié comme le cancer du poumon par Herting et Hesse dans leur enquête sur mineurs de Schneeberg, Allemagne. Les premières études d'envergure avec le radon et la santé se sont produits dans le contexte de l'extraction d'uranium dans le Région de Joachimsthal Bohême. Aux États-Unis, des études et des mesures d'atténuation ne suivis décennies d'effets sur la santé des mineurs d'uranium de la Sud-Ouest des États-Unis utilisé au début de la guerre froide ; normes ne ont pas été mises en œuvre jusqu'en 1971.
La présence de radon dans l'air intérieur a été documentée dès 1950. À partir de la recherche sur les années 1970 a été lancé pour traiter les sources de radon à l'intérieur, les déterminants de la concentration, effets sur la santé, et les approches à l'atténuation. Aux États-Unis, le problème de radon à l'intérieur a reçu une large publicité et intensifié l'enquête après un incident très médiatisé en 1984. Au cours de la surveillance de routine à une centrale nucléaire en Pennsylvanie, un travailleur a été trouvé contaminé par la radioactivité. Une contamination élevé de radon dans sa maison a ensuite été identifié comme responsable de la contamination.
Occurrence
Unités de concentration
Toutes les discussions de concentrations de radon dans l'environnement se réfèrent à 222 Rn. Alors que le taux de production moyen de 220 Rn (à partir de la série de désintégration du thorium) est environ le même que 222 Rn, la quantité de 220 Rn dans l'environnement est très inférieure à celle de 222 Rn en raison de la courte demi-vie de 220 Rn (1 minute contre 4 jours).
la concentration de radon est généralement mesurée dans l'atmosphère, en becquerel par mètre cube (Bq / m 3), le SI dérivées unité. Expositions domestiques typiques sont environ 100 Bq / m 3 à l'intérieur, et 10 à 20 Bq / m 3 à l'extérieur.
Il est souvent mesurée en picocuries par litre (pCi / L) aux Etats-Unis, avec une pCi / L = 37 Bq / m 3.
Dans l'industrie minière, l'exposition est traditionnellement mesurée en niveau (WL) de travail, et l'exposition cumulative au niveau opérationnel-mois (WLM): 1 WL égale toute combinaison de courte durée 222 Rn descendance (218 Po, 214 Pb, 214 Bi et 214 Po) dans 1 litre d'air qui libère 1,3 × 10 5 MeV d'énergie alpha potentielle; une WL est équivalent à 2,08 × 10 -5 joules par mètre cube d'air (J / m 3). L'unité SI de l'exposition cumulative est exprimée en heures-joules par mètre cube (J · h / m 3). Un WLM est équivalente à 3,6 x 10 -3 J · h / m 3. Une exposition à une WL pendant 1 mois de travail (170 heures) est égal à 1 WLM exposition cumulée.
Une exposition cumulative de 1 WLM est à peu près équivalent à vivre une année dans une atmosphère avec une concentration de radon de 230 Bq / m 3.
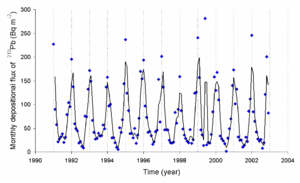
Radon (Rn 222), lorsqu'il est libéré dans l'air, se désintègre en 210 Pb et d'autres radio-isotopes, les niveaux de 210 Pb peuvent être mesurés. Le taux de dépôt de ce radio-isotope dépend des conditions météorologiques.
Les concentrations de radon trouvés dans des environnements naturels sont beaucoup trop faible pour être détectée par des moyens chimiques. A 1,000 Bq / m 3 de concentration (relativement élevé) correspond à 0,17 picogramme par mètre cube. La concentration moyenne de radon dans l'atmosphère est d'environ 6 × 10 -20 atomes de radon pour chaque molécule dans l'air, soit environ 150 atomes dans chaque ml d'air. L'activité de radon de l'atmosphère terrestre provient de quelques dizaines de grammes de radon, toujours remplacé par la décomposition de plus grandes quantités de radium et l'uranium.
Naturel
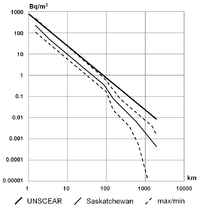
Le radon est produit par la désintégration radioactive du radium-226, qui se trouve dans les minerais d'uranium; phosphate; schistes; roches ignées et métamorphiques, comme le granit, de gneiss et de schiste; et, dans une moindre mesure, dans les roches courantes telles que le calcaire. Chaque mile carré de la surface du sol, à une profondeur de six pouces (2,6 km 2 à une profondeur de 15 cm), contient environ 1 gramme de radium, qui libère le radon en petites quantités dans l'atmosphère À l'échelle mondiale, on estime que 2400 millions curies (90 TBq) de radon sont libérés à partir du sol chaque année.
La concentration de radon varie considérablement d'un endroit à l'autre. En plein air, il varie de 1 à 100 Bq / m 3, encore moins (0,1 Bq / m 3) au-dessus de l'océan. Dans des grottes ou des mines ou gazéifiées, maisons mal aérées, sa concentration grimpe à 20-2,000 Bq / m 3. la concentration de radon peut être beaucoup plus élevé dans des contextes d'exploitation minière. réglementation de ventilation instruisent pour maintenir la concentration de radon dans les mines d'uranium dans le cadre du «niveau de travail", avec des niveaux de 95e percentile allant jusqu'à près de 3 WL (546 pCi 222 Rn par litre d'air; 20,2 kBq / m 3, mesurée 1976-1985). La concentration dans l'air à la (non ventilé) Gastein guérison Galerie moyennes 43 kBq / m 3 (1,2 nCi / L) avec une valeur maximale de 160 kBq / m 3 (4,3 nCi / L).
Radon apparaît surtout avec la chaîne de désintégration de l'radium et de l'uranium série (222 Rn), et marginalement avec la série de thorium (220 Rn). L'élément émane naturellement de la terre, et certains matériaux de construction, partout dans le monde, où des traces d'uranium ou le thorium peuvent être trouvés, et en particulier dans les régions où les sols contenant de granit ou schiste, qui ont une concentration plus élevée en uranium. Cependant, toutes les régions granitiques sont sujettes à des émissions élevées de radon. Étant un gaz rare, il migre habituellement librement à travers les défauts et les sols fragmentés, et peut se accumuler dans des grottes ou de l'eau. En raison de sa demi-vie très courte (quatre jours pour 222 Rn), la concentration de radon diminue très rapidement lorsque la distance de la zone de production augmente. La concentration de radon varie énormément avec la saison et les conditions atmosphériques. Par exemple, il a été montré à se accumuler dans l'air en cas de inversion météorologique et peu de vent.
Des concentrations élevées de radon peuvent être trouvés dans certaines eaux de source et des sources chaudes. Les villes de Boulder, Montana; Misasa; Bad Kreuznach, Allemagne ; et le pays de Japon ont ressorts de radium-riche qui émettent radon. Pour être classé comme une eau minérale de radon, la concentration de radon doit être supérieure à un minimum de 2 nCi / L (74 kBq / m 3). L'activité d'eau minérale de radon atteint 2 000 kBq / m 3 à Merano et 4000 kBq / m 3 dans Lurisia (Italie).
Les concentrations de radon naturelles dans le atmosphère de la Terre sont si bas que l'eau riche en radon en contact avec l'atmosphère sera continuellement perdre radon volatilisation. De ce fait, l'eau souterraine a une concentration plus élevée de 222 Rn que les eaux de surface, parce que le radon est produit en continu par la désintégration radioactive de 226 Ra présent dans les roches. De même, la zone saturée d'un sol a souvent une teneur en radon supérieure à la zone non saturée en raison de diffusionnelles pertes dans l'atmosphère.
En 1971, Apollo 15 a passé 110 km (68 mi) au-dessus du plateau d'Aristarque sur la Lune , et détecté une augmentation significative particules alpha pensé pour être causés par la désintégration de 222 Rn. La présence de 222 Rn a été déduit par la suite à partir de données obtenues à partir de la Lunar Prospector spectromètre de particules alpha.
On trouve du radon dans certains pétrole . Le radon a une pression similaire et la courbe de température pour le propane et les raffineries de pétrole pétrochimie distincts fondés sur leurs points d'ébullition, la tuyauterie contenant du propane fraîchement séparés dans les raffineries de pétrole peut devenir radioactifs en raison de la décomposition du radon et de ses produits.
Les résidus de pétrole et de gaz naturel industrie contiennent souvent radium et ses filles. L'échelle de sulfate d'un puits de pétrole peut être radium riche, tandis que l'eau, l'huile et le gaz d'un puits contient souvent radon. Le radon se désintègre pour former des radio-isotopes solides qui forment des revêtements à l'intérieur de la tuyauterie.
Accumulation dans les maisons

Le phénomène de contamination accrue du radon dans les maisons a été découvert par hasard en 1985 après le test rigoureux de rayonnement est effectuée à une entrée de la centrale nucléaire a révélé que Stanley Watras, un ingénieur entrer dans l'usine, a été contaminé par des substances radioactives. Expositions domestiques typiques sont d'environ 100 Bq / m 3 à l'intérieur. Selon la façon dont les maisons sont construites et ventilés, le radon peut se accumuler dans les sous-sols et les logements. Le radon peut également se infiltrer dans un environnement intérieur à travers les fissures dans les planchers solides, joints de construction, des fissures dans les murs, les lacunes dans les planchers suspendus, espaces autour des tuyaux de services, des cavités dans les murs, et l'approvisionnement en eau. Les concentrations de radon dans le même emplacement peuvent différer par un facteur de deux sur une période de 1 heure. En outre, la concentration dans une pièce d'un bâtiment peut être sensiblement différente de celle de la concentration dans une pièce voisine.
La distribution des concentrations de radon a tendance à être asymétrique autour de la moyenne: les plus grandes concentrations ont une façon disproportionnée plus de poids. La concentration de radon à l'intérieur est généralement supposée suivre une distribution log-normale sur un territoire donné. Ainsi, la moyenne géométrique est généralement utilisé pour l'estimation de la concentration de radon "moyenne" dans une zone. La concentration moyenne varie de moins de 10 Bq / m 3 à plus de 100 Bq / m 3 dans certains pays européens. Typique des écarts-types trouvés dans des études géométriques sont comprises entre 2 et 3, le sens (compte tenu de la Règle 68-95-99.7) que la concentration de radon devrait être plus d'une centaine de fois la concentration moyenne de 2 à 3% des cas.
Les plus fortes concentrations moyennes de radon dans les États-Unis se trouvent dans Iowa et dans le Zones de montagne dans le sud des Appalaches en Pennsylvanie. Certains des lectures les plus élevées ont déjà été enregistrées dans la ville irlandaise de Mallow, comté de Cork, fait craindre locales concernant le cancer du poumon. Iowa a plus fortes concentrations de radon à la moyenne des États-Unis en raison de significative glaciation qui a broyé les roches granitiques de la Bouclier canadien et déposé comme sols constituant le riches terres agricoles de l'Iowa. Beaucoup de villes dans l'Etat, tels que Iowa City, ont passé les exigences pour la construction de radon résistant dans les maisons neuves. Dans quelques endroits, résidus d'uranium ont été utilisées pour décharges et ont ensuite été construits sur, entraînant possiblement une exposition accrue au radon.
La production industrielle
Le radon est obtenu comme sous-produit de minerais uranifères traitement après le transfert en solutions à 1% de chlorhydrique ou bromhydrique. Le mélange gazeux extrait de la solution contenant H 2, O 2, He, Rn, CO 2, H 2 O et des hydrocarbures. Le mélange est purifié par passage sur de cuivre à 720 ° C pour éliminer le H 2 et le O 2, et ensuite KOH et P 2 O 5 sont utilisés pour éliminer les acides et l'humidité par sorption. Le radon est condensée par de l'azote liquide purifié à partir de gaz et de résidus par sublimation.
Radon commercialisation est réglementée, mais il est disponible en petites quantités pour l'étalonnage des 222 systèmes de mesure Rn, à un prix de près de $ 6000 par millilitre de solution de radium (qui ne contient environ 15 picogrammes de radon réelle à un moment donné). Le radon est produit par une solution de radium-226 (demi-vie de 1600 ans). Le radium-226 se désintègre par émission de particules alpha, la production de radon qui se accumule sur des échantillons de radium-226 à une vitesse d'environ 1 mm 3 / jour et par gramme de radium; l'équilibre est rapidement atteint et le radon est produit dans un flux continu, avec une activité égale à celle du radium (50 Bq). Rn gazeux 222 (demi-vie d'environ quatre jours) se échappe de la capsule par diffusion.
échelle de concentration
| Bq / m 3 | pCi / L | exemple de Présence |
|---|---|---|
| 1 | ~ 0,03 | La concentration de radon sur les rives des grands océans est typiquement de 1 Bq / m 3. Concentration de trace Radon-dessus des océans ou dans l'Antarctique peut être inférieur à 0,1 Bq / m 3. |
| 10 | 0,27 | Concentration moyenne continentale à l'air libre: de 10 à 30 Bq / m 3. Basé sur une série d'enquêtes, la concentration globale moyenne du radon est estimé à 39 Bq / m 3. |
| 100 | 2,7 | Exposition domestique intérieure typique. La plupart des pays ont adopté une concentration de radon de 200 à 400 Bq / m 3 pour l'air intérieur comme une action ou des niveaux de référence. Si le test montre des niveaux inférieurs à 4 picocuries radon par litre d'air (150 Bq / m 3), aucune action ne est nécessaire. Une exposition cumulée de 230 Bq / m 3 de la concentration de radon au cours d'une période de 1 an correspond à une WLM. |
| 1000 | 27 | Concentrations de radon très élevés (> 1 000 Bq / m 3) ont été trouvés dans des maisons construites sur des sols à haute teneur d'uranium et / ou de haute perméabilité du sol. Si les niveaux sont de 20 picocuries radon par litre d'air (800 Bq / m 3) ou plus, le propriétaire de la maison devrait envisager un certain type de procédure pour réduire les niveaux de radon à l'intérieur. |
| 10000 | 270 | Le "niveau de travail" dans les mines d'uranium correspond à une 7,000 Bq / m 3 la concentration. La concentration dans l'air à les (non ventilés) Gastein guérison Galerie moyennes 43 kBq / m 3 (environ 1,2 nCi / L) avec une valeur maximale de 160 kBq / m 3 (environ 4,3 nCi / L). |
| 100000 | ~ 2700 | A propos de 100 000 Bq / m 3 (2,7 nCi / L) a été mesurée dans Le sous-sol de Stanley Watras. |
| 1000000 | 27000 | Les concentrations atteignant 1.000.000 Bq / m 3 peuvent être trouvés dans les mines d'uranium non ventilés. |
Applications
Médical
Une forme du début du 20e siècle charlatanisme était le traitement des maladies dans un radiotorium. Ce était une petite pièce scellée pour les patients d'être exposés au radon pour ses "effets médicinaux". Le caractère cancérigène du radon en raison de son rayonnement ionisant est apparu plus tard. Molécule endommager la radioactivité du radon a été utilisé pour tuer les cellules cancéreuses. Il n'a pas, cependant, augmenter la santé des cellules saines. En fait, le rayonnement ionisant provoque la formation de radicaux libres, ce qui entraîne des dommages aux cellules génétiques et autres, ce qui entraîne une augmentation des taux de la maladie, y compris le cancer .

L'exposition au radon, un processus connu sous le nom hormèse de rayonnement, a été proposé pour atténuer les maladies auto-immunes telles que l'arthrite. En conséquence, à la fin du 20ème siècle et début du 21e siècle, "mines de santé» établies dans Basin, Montana a attiré des gens qui demandent un allégement de problèmes de santé comme l'arthrite travers une exposition limitée à l'eau de la mine radioactifs et le radon. Cependant, la pratique est déconseillée en raison des effets nocifs bien documentés de fortes doses de rayonnement sur le corps.
Bains d'eau radioactives ont été appliquées depuis 1906 dans Jáchymov, République tchèque , mais avant même la découverte de radon, ils ont été utilisés dans les Bad Gastein, en Autriche . ressorts de Radium-riches sont également utilisés dans traditionnelle japonaise onsen dans Misasa, Préfecture de Tottori. Traitement potable est appliquée dans Bad Brambach, Allemagne . La thérapie par inhalation est réalisée en Gasteiner-Heilstollen, en Autriche, en Świeradów-Zdrój, Czerniawa-Zdrój, Kowary, Ladek Zdroj, en Pologne, en Harghita Bai, Roumanie, et Boulder, États-Unis. Aux États-Unis et en Europe il ya plusieurs "radon spas », où les gens se assoient pour les minutes ou heures dans une atmosphère de haute radon dans la croyance que de faibles doses de rayonnement seront tonifier ou stimuler eux.
Le radon a été produit commercialement pour une utilisation en radiothérapie, mais la plupart du temps a été remplacé par des radionucléides effectués dans les accélérateurs et les réacteurs nucléaires. Le radon a été utilisé dans les semences implantables, en or ou en verre, principalement utilisé pour traiter les cancers. Les graines d'or ont été produites par le remplissage d'un tube long de radon pompée depuis une source de radium, le tube étant ensuite divisé en petites sections par sertissage et de coupe. La couche d'or maintient le radon à l'intérieur, et filtre les rayonnements alpha et bêta, tout en permettant la rayons gamma se échapper (qui tuent le tissu malade). Les activités peuvent aller de 0,05 à 5 millicuries par graine (2-200 MBq). Les rayons gamma sont produits par le radon et les premiers éléments de courte durée de sa chaîne de décroissance (218 Po, 214 Pb, 214 Bi, 214 Po).
Le radon et ses produits de désintégration premier étant très courte durée, la graine est laissé en place. Après 12 demi-vies (43 jours), la radioactivité du radon est à 1/2000 de son niveau d'origine. A ce stade, l'activité résiduelle prédominante provient de la des descendants du radon 210 Pb, dont la demi-vie (22,3 années) est 2000 fois supérieure à celle de radon (et dont l'activité est donc 1/2000 du radon de), et ses descendants 210 Bi et 210 Po, totalisant 0,03% de l'activité initiale des semences.
Dans la première partie du 20ème siècle aux Etats-Unis, l'or contaminés par 210 Pb entré dans l'industrie de bijoux. Ce était à partir de graines d'or qui avaient tenu 222 Rn qui avait été fondu après la radon avait pourri.
Scientifique
Émanation du radon du sol varie avec le type de sol et teneur en uranium de surface, donc les concentrations de radon en plein air peut être utilisé pour suivre les masses d'air à un degré limité. Ce fait a été mis à profit par certains scientifiques atmosphériques. En raison de la perte rapide de radon à l'air et de la décomposition relativement rapide, le radon est utilisé dans hydrologique recherche qui étudie l'interaction entre les eaux souterraines et ruisseaux. Une concentration importante de radon dans un flux est un bon indicateur qu'il ya intrants locaux de l'eau souterraine. Le radon est également utilisé dans la datation des sols contenant de l'huile parce que le radon a une forte affinité pour les substances analogues aux hydrocarbures.
Radon sol concentration a été utilisé de façon expérimentale à map enterré gros souterraines géologiques défauts parce que les concentrations sont généralement plus élevés au cours des défauts. De même, il a trouvé une utilisation limitée dans la prospection pour gradients géothermiques.
Certains chercheurs ont étudié l'évolution des concentrations de radon pour les eaux souterraines la prévision des séismes. Le radon a une demi-vie d'environ 3,8 jours, ce qui signifie qu'il peut être constaté que peu de temps après qu'il a été produit dans la chaîne de désintégration radioactive. Pour cette raison, il a été émis l'hypothèse que l'augmentation de la concentration de radon est due à la génération de nouvelles fissures souterraines, ce qui permettrait une meilleure circulation de l'eau souterraine, débusquer radon. La génération de nouvelles fissures pourrait ne pas déraisonnablement supposer précéder grands tremblements de terre. Dans les années 1970 et 1980, des mesures scientifiques d'émissions de radon près de défauts constaté que les tremblements de terre se produisent souvent sans signal de radon, et le radon a été souvent détectés sans tremblement de terre à suivre. Il a ensuite été rejeté par beaucoup comme un indicateur fiable. Cependant, à partir de 2009, il est sous enquête comme un précurseur possible par la NASA.
Le radon est un polluant connu émis par centrales géothermiques, mais il se disperse rapidement, et aucun risque radiologique a été démontrée dans diverses enquêtes. La tendance dans les centrales géothermiques est de réinjecter la totalité des émissions par pompage à grande profondeur, et cela semble susceptible de diminuer en fin de compte ces risques radon plus loin.
Dans les années 1950, le radon a été utilisé dans l'industrieradiographie.
Risques pour la santé - radon dans l'air
Le radon dans les mines
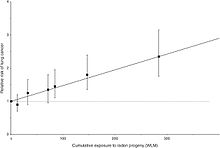
Radon-222 (de descendance effectivement radon) a été classé par l'Agence Internationale pour la Recherche sur le Cancer comme étant cancérigène pour les humains, et comme un gaz qui peut être inhalée, le cancer du poumon est une préoccupation particulière pour les personnes exposées à des niveaux élevés de radon pendant des périodes prolongées de temps. Pendant les années 1940 et 50, lorsque les normes de sécurité nécessitant une ventilation coûteux dans les mines ont pas été largement mises en œuvre, l'exposition au radon a été liée au cancer du poumon chez les mineurs non-fumeurs de l'uranium et d'autres matériaux de hard rock dans ce qui est maintenant la République tchèque , et plus tard chez les mineurs du sud des États-Unis.
Depuis ce temps, de ventilation et d'autres mesures ont été utilisés pour réduire les niveaux de radon dans les mines les plus touchés qui continuent à fonctionner. Au cours des dernières années, l'exposition annuelle moyenne des mineurs d'uranium a chuté à des niveaux similaires aux concentrations inhalées dans certaines maisons. Cela a réduit le risque de cancer d'origine professionnelle au radon, bien que les problèmes de santé peuvent persister pour ceux qui ont actuellement un emploi dans les mines concernées et pour ceux qui ont été employés en eux dans le passé. Comme le risque relatif pour les mineurs a diminué, a donc la capacité de détecter les excès de risque parmi cette population.
De nombreux chercheurs ont mis en évidence une augmentation possible du risque théorique dela leucémie du radon, mais le soutien empirique pour ce qui n'a pas vu le jour.
Exposition au niveau national
exposition au radon (en fait de filiation du radon) a été liée au cancer du poumon dans de nombreuses études cas-témoins réalisées aux États-Unis, en Europe et en Chine. Il ya environ 21 000 décès par an aux Etats-Unis en raison de cancers pulmonaires induits par le radon.
L'une des études les plus complètes réalisées radon aux États-Unis par le Dr R. William terrain et ses collègues ont constaté un risque accru de cancer du poumon de 50%, même dans les expositions prolongées au niveau de l'action de l'EPA de 4 pCi / L. Amérique du Nord et en gestion commune européenne analyses soutiennent encore ces conclusions.
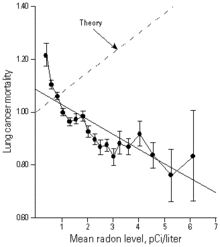
La plupart des modèles d'exposition au radon résidentiel sont basées sur des études de mineurs, et les estimations directes des risques pour les propriétaires serait plus souhaitable. Néanmoins, en raison de la difficulté de mesurer le risque de radon par rapport à d'autres contributeurs savoir-fumeur modèles de leur effet ont souvent fait usage d'entre eux.
Le radon a été considérée comme la deuxième cause de cancer du poumon et principale cause environnementale de mortalité par cancer par les Environmental Protection Agency des États-Unis. autres ont abouti à des conclusions similaires pour le Royaume-Uni et la France. L'exposition au radon dans les maisons et bureaux peut provenir de certaines formations rocheuses souterraines, et aussi de certains matériaux de construction (par exemple, certains granites). Le plus grand risque d'exposition au radon se pose dans des bâtiments étanches à l'air, insuffisamment aéré, et avoir des fuites de base qui permettent à l'air de la terre dans les sous-sols et les pièces d'habitation.
Le radon et le tabagisme
Les résultats des études épidémiologiques indiquent que le risque de cancer du poumon augmente avec l'exposition au radon résidentiel. Cependant, il ya toujours de grandes incertitudes dans ces études. Un exemple classique et bien connu de la source d'erreur est le tabagisme. En outre, le tabagisme est le facteur de risque le plus important pour le cancer du poumon. Dans l'Ouest, on estime la fumée de tabac à la cause d'environ 90% de tous les cancers du poumon. Il ya une tendance pour les autres risques de cancer du poumon hypothétiques se noient dans le risque de tabagisme. Les résultats des études épidémiologiques doivent toujours être interprétés avec prudence.
Selon l'EPA, le risque de cancer du poumon chez les fumeurs est important en raison des effets synergiques de radon et le tabagisme. Pour cette population d'environ 62 personnes dans un total de 1 000 mourront du cancer du poumon par rapport à 7 personnes dans un total de 1000 pour les personnes qui ont jamais fumé. Il ne peut cependant pas être exclu que le risque de non-fumeurs devrait être expliquée principalement par un effet de combinaison de radon et le tabagisme passif (voir ci-dessous).
Le radon, comme d'autres facteurs de risque externes connus ou suspectés de cancer du poumon, est une menace pour les fumeurs et les anciens fumeurs. Cela a été clairement démontré par l'étude de la mise en commun européen. Un commentaire de l'étude de mise en commun, a déclaré: "il ne convient pas de parler simplement d'un risque de radon dans les maisons Le risque est de fumer, aggravée par un effet synergique du radon pour les fumeurs sans fumer, l'effet semble être si petit.. à être insignifiant ».
Une étude du rayonnement depuis post mastectomie radiothérapie montre que les modèles simples utilisés précédemment pour évaluer les risques combinés et séparés de rayonnement et le tabagisme doivent être développées. Ceci est également soutenu par la nouvelle discussion sur la méthode de calcul, LNT, qui a toujours été utilisés.
Le radon et le tabagisme passif
Une question importante est de savoir si le tabagisme passif peut également provoquer un effet de synergie similaire avec le radon résidentiel. Ce n'a pas été suffisamment étudiée. Les données de base pour l'étude de la mise en commun européen, il est impossible d'exclure qu'un tel effet de synergie est une explication de l'augmentation (très limitée) dans le risque du radon qui a été déclaré pour les non-fumeurs.
Une étude de 2001, qui comprenait 436 cas (les non-fumeurs qui ont eu le cancer du poumon), et un groupe de contrôle (1649 jamais des fumeurs) ont montré que l'exposition au radon augmente le risque de cancer du poumon chez les non-fumeurs. Mais le groupe qui avaient été exposés au tabagisme passif à la maison semblait supporter l'augmentation des risques ensemble, tandis que ceux qui ont pas été exposés au tabagisme passif ne démontraient pas de risque accru avec l'augmentation de la concentration de radon.
Ce résultat doit confirmation par des études supplémentaires. Malgré les résultats surprenants de 2001, de nouvelles études semblent pas avoir été mises en œuvre.
Risques pour la santé - radon dans l'eau potable
Les effets du radon si ingérés sont tout aussi inconnue, bien que des études ont montré que sa demi-vie biologique varie de 30 à 70 minutes, avec 90 pour cent retrait à 100 minutes. En 1999, Conseil national de recherches a étudié la question de radon dans l'eau potable. Les risques associés à l'ingestion a été considéré presque négligeable.
En plus d'être ingéré par l'eau potable, le radon est également libéré de l'eau lorsque la température augmente, la pression diminue et lorsque l'eau est aérée. Les conditions optimales pour le radon libération et l'exposition se produisent pendant la douche. Eau avec une concentration de radon de 10 4 pCi / L peut augmenter la concentration de radon dans l'air intérieur par 1 pCi / L dans des conditions normales d'utilisation de l'eau.
Les concentrations de radon dans l'air peuvent être élevés dans les plantes avec de grandes piscines d'eau souterraine, comme les usines de traitement d'eau potable.
Tests et mesures d'atténuation

Selon "Un citoyen Guide de Radon" de l'EPA, la méthode pour réduire le radon "... principalement utilisé est un système de conduit d'évacuation et d'un ventilateur, ce qui tire le radon de sous la maison et les évents à l'extérieur», qui est aussi appelé dépressurisation sous la dalle, dépressurisation active du sol, ou la succion du sol. Généralement radon à l'intérieur peut être atténué par dépressurisation sous la dalle et épuisant tel air de radon chargé à l'extérieur, loin des fenêtres et autres ouvertures du bâtiment. "EPA recommande généralement des méthodes qui empêchent l'entrée du radon. Aspiration du sol, par exemple, empêche le radon de pénétrer dans votre maison en tirant le radon sous la maison, et son évacuation à travers un tuyau ou des tuyaux, à l'air au-dessus de la maison où il est rapidement diluée "et" EPA ne recommande pas l'utilisation d'étanchéité seule à réduire le radon parce que, par lui-même, étanchéité n'a pas été montré pour réduire les niveaux de radon de manière significative ou constante ", selon l'EPA" Guide du consommateur à la réduction de Radon: Comment réparer ta maison ".
Les systèmes de ventilation en pression positive peuvent être combinés avec un échangeur de chaleur pour récupérer l'énergie dans le processus d'échange d'air avec l'extérieur, et d'épuiser tout simplement l'air du sous-sol à l'extérieur est pas nécessairement une solution viable, car cela peut effectivement tirer des gaz radon dans une habitation. Les maisons construites sur un vide sanitaire peuvent bénéficier d'un collecteur de radon installé sous une «barrière de radon" (une feuille de plastique qui recouvre le vide sanitaire). Pour les vides sanitaires, l'EPA indique "Une méthode efficace pour réduire les niveaux de radon dans les maisons de vide sanitaire consiste à recouvrir le sol de la terre avec une feuille de plastique haute densité. Un tuyau de ventilation et le ventilateur sont utilisés pour aspirer le radon sous la feuille et de ventilation à la à l'extérieur. Cette forme de succion du sol est appelé aspiration sous-membranaire, et lorsqu'il est correctement appliqué est le moyen le plus efficace pour réduire les niveaux de radon dans les maisons de vide sanitaire ".
